Hay muchos tipos de membranas celulares. Son algo más que sistemas de la célula:
- Forman o aíslan compartimentos cerrados.
- Regulan el paso o movimientos de sustancias a través de ellas.
- Se encargan del paso de información: las membranas tienen receptores específicos de un ligando.
- Se encargan del reconocimiento intercelular.
- Son la plataforma donde se van a ordenar los componentes de un determinado proceso.
- Se encargan de transducciones de energía y transformaciones de energía.
- Participan en la transmisión del impulso nervioso.
- Se encargan de la absorción de sustancias.
- Etc.
Todas las membranas estudiadas tienen una estructura semejante, con una composición de alrededor de un 40% de lípidos y un 60% de proteínas, pudiendo llegar a estar incluso invertidos estos datos, es decir, 60% de lípidos y 40% de proteínas.
En muchos casos aparecen hidratos de carbono unidos a los lípidos o a las proteínas.
El principal componente en cuanto a lípidos son los fosfolípidos, suponiendo un 55% o más. Los más frecuentes son los derivados de la glicerina. Pero otros fosfolípidos dependen de otros alcoholes.
Los fosfolípidos son moléculas antipáticas es decir, que poseen una parte hidrófila y una parte hidrófoba.
La parte hidrófoba está constituida las dos colas hidrocarbonadas, formadas por los ácidos grasos.
Y una parte hidrófila, formada por la cabeza. En esta cabeza tendremos un ácido fosfórico al que se enlazará, normalmente, un alcohol variable.
 |
| Fosfolípido. |
Muchas membranas tienen muchos tipos de fosfolípidos. Por ejemplo, en algunas aparecen los esfingolípidos, que son lípidos que derivan de la esfingosina. En los esfingolípidos el grupo polar estará constituido por algún hidrato de carbono. Es decir, las dos moléculas hidrófobas provienen, una de la esfingosina y otra del ácido graso.
 |
| Esfingolípido. |
Los fosfolípidos se representan esquemáticamente de la siguiente manera.
 |
| Esquema de un fosfolípido. |
Un tercer componente en las membranas plasmáticas de las células eucariotas es el colesterol. Es un esteroide.
 |
| Colesterol. |
Todos los que hemos visto todos estos componentes son anfipáticos. Esto es el responsable de su función estructural en las membranas celulares. Las moléculas anfipáticas, cuando se encuentran en agua, tienden a colocarse de modo que las partes hidrófobas se asocien y se alejen del agua. Las hidrófilas hacen frente al agua. Esto se puede conseguir de dos maneras: formando micelas o formando bicapas.
 |
| Micelas y bicapas. |
Para los fosfolípidos y glucolípidos, la estructura más estable es la bicapa. Se adaptan espontáneamente. Las bicapas forman vesículas. Se les llama liposomas. Las fuerzas que las estabilizan son las interacciones hidrófobas entre las colas y las interacciones de Van der Wallas al estar muy cerca. Por otro lado, las cabezas polares pueden formar puentes de hidrógeno o puentes salinos con el medio acuoso.
 |
| Esquema: proteína de membrana. |
Las proteínas de membrana son globulares. Se pueden separar en dos grupos: hidrosolubles, que se separan con facilidad, o antipáticas, con una parte hidrófoba. Las proteínas que tienen una parte hidrófoba y son antipáticas se les llama integrales. Tienen una conformación inversa a las normales, con los grupos apolares hacia fuera en vez de hacia adentro.
Las dos caras de la membrana, internas y externas, no tienen porque ser idénticas. En los animales hay una parte que se denomina glicocáliz. Puede, además, haber interrupciones, partes más o menos gruesas o densas.
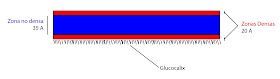 |
| Proteina con glicocalix. |
Modelo del mosaico fluido.
Fue propuesta por Singer y Nicolson en 1972. Las membranas son soluciones bidimensionales de lípidos y proteínas orientados:
La bicapa lipídica crea una barrera en la que se asientan las proteínas. Las dos capas densas están formadas por las partes hidrófilas. La capa intermedia está formada por la parte hidrófoba.
 |
| Membrana |
Las proteínas periféricas son hidrófilas. Se unen a la membrana por interacciones hidrofílicas con las cabezas de los lípidos o a las partes hidrófilas de las proteínas integrales.
Las proteínas integrales están unidas a la bicapa lipídica. Son en gran parte hidrófobas. Están sujetas por interacción hidrófoba.
Dentro de las proteínas integrales las hay transmembrana, si la atraviesan de parte a parte. Es frecuente que se formen en las integrales, poros hidrófobos.
No hay enlaces covalentes. Se basa en la cooperación de muchos enlaces débiles.
Los hidratos de carbono siempre están hacia el exterior, nunca hacia el citoplasma.
Las membranas son asimétricas. Una de estas asimetrías es la disposición de los árboles de azúcares, que como acabamos de decir están solo en una de las caras de la membrana. En el caso de la membrana plasmática, ya indicamos que están hacia el exterior. Cuando están muy desarrollados, los árboles son muy grandes, hablamos de glucocálix. En las membranas internas, como el aparato de Golgi, o en vesículas interiores, los azúcares se sitúan hacia la cara interior o luminar de las mismas.
En las células, en el interior de cloroplastos o mitocondrias, no hay hidratos de carbono. En las bacterias, a veces, los lípidos de una monocapa no corresponden con el de la otra monocapa.
Los fosfolípidos tampoco son simétricos. En la membrana de los eritrocitos, en la cara exterior, encontramos fundamentalmente fosfatidilcolina. En la interior hay otros fosfolípidos.
Las proteínas transmembrana tienen una orientación fija, siempre es la misma. En el eritrocito, la glicoforina siempre se coloca de la misma manera.
 |
| Esquema: proetínas de membrana. |
Las proteínas de membrana se sintetizan en los ribosomas que están pegados a la membrana. La conformación tiene que ver con el transporte a través de la membrana.
Fluidez de la membrana.
Otra propiedad importante de las membranas será su fluidez. Por una parte está la fluidez de los propios lípidos. Tienen varios tipos de movimientos dentro de la bicapa.
Los lípidos se pueden desplazar rápidamente dentro de una misma monocapa y conservando su orientación.
 |
| Movimientos de los lípidos de membrana. |
Hay factores que influyen en la fluidez de la membrana. A más temperatura, más fluidez y viceversa. Se habla de temperatura de transición, que sería la temperatura en la que la membrana pasa de tener una consistencia líquida a pasa a una consistencia de gel cristalino. Cada membrana tendrá su propia temperatura de transición.
Otros factores serán los factores de composición. Son fundamentalmente tres:
- Grado de saturación de los ácidos grasos. Cuando hay un mayor número de ácidos grasos con dobles enlaces, la cadena hace quiebros, las colas tienen dobleces en lugar de ir rectas, provocándose huecos. Esto hace que la membrana sea más fluida y su temperatura de transición más baja.
- Ácidos grasos de cadena corta. Se dificulta el empaquetamiento por lo que la membrana se hace más fluida. Al igual que en el caso anterior, se crean huecos que provocan que las fuerzas de Van der Waals sean menos efectivas.
- Presencia de colesterol: solo aparece en eucariotas, nunca en procariotas. Modula la fluidez. A temperatura alta, el colesterol evita el exceso de fluidez. Y viceversa, cuando la temperatura es baja, evita la cristalización. Hace un efecto de unión, acerca las moléculas. Por otro lado, separa las moléculas disminuyendo la fluidez. Es decir, depende de como se coloque. Hace que los cambios de temperatura no se hagan sentir en exceso.
 |
| Colesterol y fluidez de membrana. |
Las proteínas también se mueven. Se desplazan en el plano de la membrana, o rotan. Parece que no pueden cambiar de una monocapa a la otra.
Hay dos factores que modulan la rapidez con la que se mueven. Por un lado, la fluidez de la bicapa. Por otro, el tamaño o peso molecular de la proteína. Si tiene un peso molecular elevado, se mueve más despacio.
Las proteínas, según esto, se deberían mover más de o que en realidad se mueve. Esto se debe a una serie de factores que restringen el movimiento.
Por un lado, puede deberse a la asociación de varias proteínas que formarán complejos.
 |
| Complejos protéicos de membrana. |
Por otro lado, tenemos la unión a proteínas periféricas que las unirán entre si indirectamente. Esto se conoce muy bien en los eritrocitos. Esto, además, puede ser usado para mantener la forma de la célula, funcionando como un esqueleto.
 |
| Esqueletos proéticos de membrana. |
Un tercer tipo, relacionado con el anterior, es la unión a proteínas del citoesqueleto.